今回は製薬会社アムジェン(AMGN)の中長期の経営戦略についての分析です。
詳細な分析はアボマガ・エッセンシャルの配信記事に書いています。ここでは分析の一部を切り取って配信します。
米国でのヒュミラバイオシミラー市場でシェアを取れるか
アムジェンの今後の成長ドライバーの一つとなるのはバイオシミラー分野です。
バイオシミラーについて、アムジェンは来年1月31日にアッヴィのブロックバスター薬であるヒュミラのバイオシミラーであるアムジェビタを米国で販売します。2016年にすでに米FDAから承認済みで、米国で販売される最初のヒュミラのバイオシミラーとなります。
バイオシミラーは特許という堀がなく、激しい競争に晒されることになるので、アムジェンがどこまで売上を伸ばせるかどうかは未知数です。
ヒュミラのバイオシミラー市場では、サンドズ、サムスン・バイオジェンといった企業との競争に晒されます。
ただ、バイオシミラーはジェネリック医薬品と違い、生物由来であるため組成が複雑で、先発バイオ医薬品と同一なものがつくれません。有効性や安全性が先発薬よりも劣る可能性が、ジェネリック医薬品と比べて大きいとみなされています。
そのためバイオシミラーではジェネリック医薬品以上に信頼の大きさがカギを握ります。またバイオシミラーの開発・生産には多額の資本が必要です。
よってバイオテクノロジー業界で長期間の実績がある大企業が有利になりやすいと考えられます。
アムジェンはバイオテクノロジー業界のパイオニアであり、40年間市場をリードしてきた実績に基づく信頼があり、ブランド力があるため、バイオシミラー市場でトップリーダーになれる潜在性はあるでしょう。
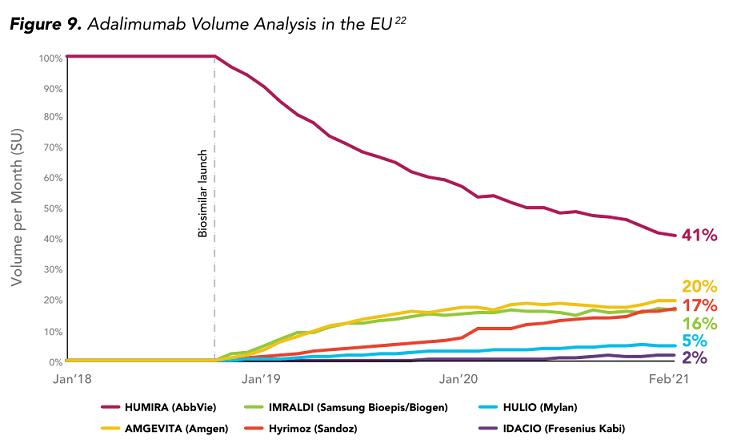
ヒュミラのバイオシミラーは2019年にEUで先行販売しています。下図をみると、アムジェン、サンドズ、サムスン・バイオジェンという大企業が多くのシェアを持ち競争力が高いことがわかります。
そのなかでアムジェンはヒュミラ市場で20%のシェアを持ち、バイオシミラーのなかで最大のシェアを持ちます。
アムジェビカは米国で最初に市場に投入され、およそ半年間にわたって先行者利益を得られます。米国でも有利に展開できるのではないでしょうか。
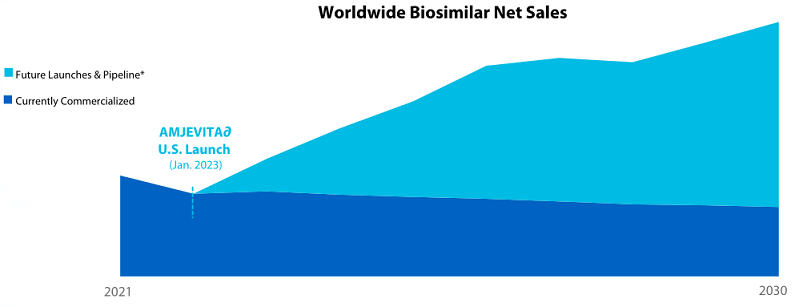
米国のバイオシミラー市場はEUなどと比べて展開が遅れていましたが、2015年に登場して以来市場規模は拡大し、保険適用の拡大も進んできました。
薬価が上昇し、患者だけでなく米国政府の公的医療保険の支出が増え続け今後も財政を圧迫していくので、バイオシミラー市場の拡大は待ったなしの状況となっています。
アムジェンがバイオシミラーでどの程度成長できるかどうかは現時点で判断できませんが、市場が拡大する中で、これまでのアムジェンの実績やブランド力から有利な位置にいることはおそらく間違いないでしょう。
ヒュミラは2014年以来8年連続で世界で最も売れた薬剤であり、昨年の売上は207億ドルでした。これは昨年のアムジェンの薬剤からの年間売上の85%にものぼります。
バイオシミラーなので価格はヒュミラの数分の一になりますが、ある程度のシェアを米国で獲得できればアムジェンの業績をそれなりに押し上げていきます。
期待の2つの新薬、一つは見通し良好だが一つは視界不良
新薬のうち、現時点である程度の成長を期待しても良さそうなのは、重度の喘息患者向け治療薬であるテゼペルマブです。昨年末に米FDAから承認されました。
非好酸球型の患者にも有効であり、病因によらずどの重度の喘息患者にも有効な現状唯一の治療薬という強みを活かして、売上を伸ばしていくことになります。
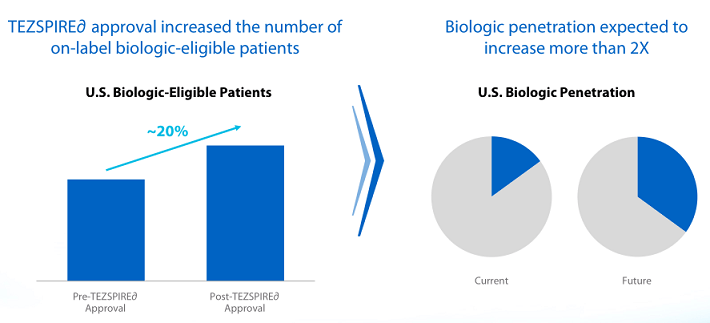
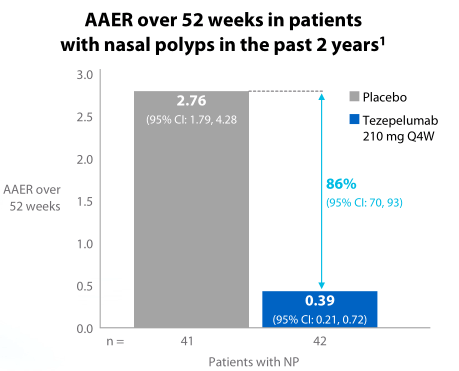
テゼペルマブは他にも鼻ポリープを伴う慢性副鼻腔炎、好酸球性食道炎、慢性の自発性蕁麻疹、慢性閉塞性肺疾患への適応拡大を目指し治験を行っています。
鼻ポリープを伴う慢性副鼻腔炎の治験ではプラセボと比べて圧倒的な有効性を示しています。
いまのところ、テゼベルマブの開発は順調に進んでいるようです。
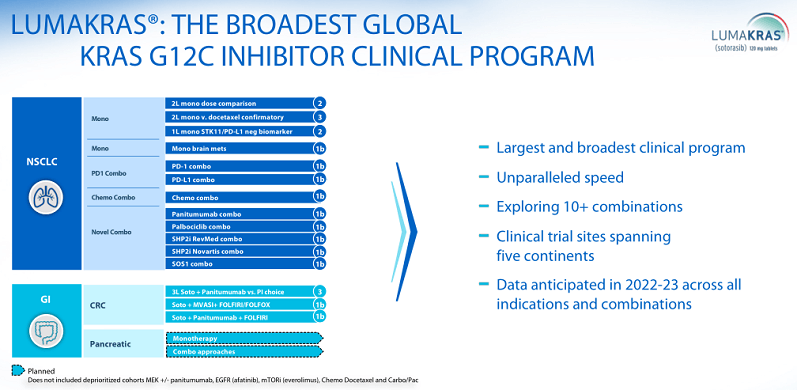
現時点で収益拡大が未知数なのが、KRAS阻害薬の抗がん剤であるルマクラスです。
非小細胞肺がん患者向けに米国、EU、日本で迅速承認を受け、条件付きで上市しています。現在フェーズ4治験中で、有効なデータが出てくれば正式に承認となります。
フェーズ4治験の結果公表は当初、今年上半期の予定でしたが、下半期に先延ばしとなりました。
ルマクラスのシェア拡大を阻む障害は競争です。といってもKRAS阻害薬同士の競争はいまのところ、市場が心配するほどの問題ではなさそうです。
KRAS阻害薬の最大のライバルはミラティのAgenusですが、アムジェンが1年開発で先行しており、ミラティは財務が厳しく、Agenusの治験結果公表が遅れると承認が厳しくなるという状況に置かれています。
ルマクラスのフェーズ4治験結果の公表が先送りされたことはミラティに与える圧力を和らげることになりますが、アムジェンの競争優位な状況を脅かするものではありません。
問題は、キイトルーダをはじめとした免疫チェックポイント療法などとの競争です。
KRAS阻害薬は免疫チェックポイント阻害薬と作用機序が異なり、経口薬のため、単剤としては差別化できていると考えられます。
しかしキイトルーダなどと併用した場合に、独自の有効性を得られるのかどうか不透明です。差別化できなければ、ルマクラス併用療法の需要は高まらず、次々と併用療法が適応承認され信頼をますます集めているキイトルーダという壁がルマクラスの普及を妨げます。
今年から来年にかけて、ルマクラス併用療法の治験結果が次々と出てきます。他のがん治療法と比べた有効性・安全性での優位点・差別点が見いだせるのかが、成長に必要となります。